Vanillinglucosid
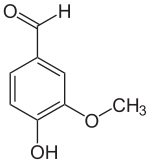
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||
| Allgemeines | |||||||||||||
| Name | Vanillinglucosid | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C14H18O8 | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 314,29 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||
| Schmelzpunkt |
189 °C[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Vanillinglucosid (auch Vanillosid oder Glucovanillin) ist das natürlich vorkommende Glucosid des Vanillins. Vor der Fermentation von Vanilleschoten liegt das Vanillin hauptsächlich als Vanillinglucosid vor.
Vorkommen und Biosynthese
[Bearbeiten | Quelltext bearbeiten]
Grüne, unfermentierte Vanilleschoten der Orchidee Vanilla planifolia weisen nicht den charakteristischen Vanillegeschmack auf, da das Vanillin fast ausschließlich in Form von Vanillinglucosid vorliegt. Bei der Fermentation wird die glycosidische Bindung durch β-Glucosidase gespalten und das Vanillin freigesetzt.[2][3] Die Biosynthese ist nicht im Detail aufgeklärt, allerdings gibt es schon länger deutliche Indizien, die dafürsprechen, dass Ferulasäure ein biosynthetisches Intermediat ist. Ein anderes mögliches Intermediat ist das Loroglossin,[S 1] eine Verbindung die aus zwei Molekülen glucosidiertem 4-Hydroxybenzylalkohol[S 2] besteht, die mit Weinsäure verestert sind.[2] In einer im Jahr 2014 publizierten Studie wurde gezeigt, dass die Vanillin-Synthase die Umwandlung von Ferulasäure bzw. deren Glucosid zu Vanllin bzw. Vanillinglucosid katalysiert.[4]
Herstellung
[Bearbeiten | Quelltext bearbeiten]Vanillinglucosid kann biotechnologisch durch modifizierte Hefepilze (Saccharomyces cerevisiae) hergestellt werden. Dabei wird 3-Dehydroshikimisäure[S 3] aus dem Shikimisäure-Weg zunächst zu Protocatechusäure umgesetzt. Diese wird über Vanillinsäure oder Protocatechualdehyd zunächst zu Vanillin umgesetzt, das zuletzt zu Vanillinglucosid glycosyliert wird.[5]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d Datenblatt Glucovanillin bei Sigma-Aldrich, abgerufen am 15. Februar 2024 (PDF).
- ↑ a b Nicholas J. Walton, Melinda J. Mayer, Arjan Narbad: Vanillin. In: Phytochemistry. Band 63, Nr. 5, Juli 2003, S. 505–515, doi:10.1016/S0031-9422(03)00149-3.
- ↑ Anish Kundu: Vanillin biosynthetic pathways in plants. In: Planta. Band 245, Nr. 6, Juni 2017, S. 1069–1078, doi:10.1007/s00425-017-2684-x.
- ↑ Nethaji J. Gallage, Esben H. Hansen, Rubini Kannangara, Carl Erik Olsen, Mohammed Saddik Motawia, Kirsten Jørgensen, Inger Holme, Kim Hebelstrup, Michel Grisoni, Birger Lindberg Møller: Vanillin formation from ferulic acid in Vanilla planifolia is catalysed by a single enzyme. In: Nature Communications. Band 5, Nr. 1, 19. Juni 2014, doi:10.1038/ncomms5037, PMID 24941968, PMC 4083428 (freier Volltext).
- ↑ Tomas Strucko, Olivera Magdenoska, Uffe H Mortensen: Benchmarking two commonly used Saccharomyces cerevisiae strains for heterologous vanillin-β-glucoside production. In: Metabolic Engineering Communications. Band 2, Dezember 2015, S. 99–108, doi:10.1016/j.meteno.2015.09.001, PMID 34150513, PMC 8193238 (freier Volltext).
Anmerkungen
[Bearbeiten | Quelltext bearbeiten]- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Loroglossin: CAS-Nummer: 58139-22-3, PubChem: 185907, Wikidata: Q82957739.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 4-Hydroxybenzylalkohol: CAS-Nummer: 623-05-2, EG-Nummer: 210-768-0, ECHA-InfoCard: 100.009.790, PubChem: 125, ChemSpider: 122, Wikidata: Q5526828.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 3-Dehydroshikimisäure: CAS-Nummer: 55-73-2, EG-Nummer: 634-499-7, ECHA-InfoCard: 100.162.474, PubChem: 439774, ChemSpider: 388830, DrugBank: DB04347, Wikidata: Q3604487.